让癌细胞“起内讧”!科学家提出肿瘤新疗法 解决癌症复发转移痛点
图:工程癌细胞(绿色)向脑肿瘤细胞(红色)传递一种治疗分子。
(图源:Khalid Shah laboratory)
癌细胞具有自主移动的能力:它们可以在身体周围移动以定位肿瘤。
在转移性肿瘤中,当转移灶形成后,原发部位就会源源不断地输送新的癌细胞,这一过程又被称作癌细胞自主归巢。
对于癌症,目前有许多治疗手段,如切除、放疗和化疗,但都难以解决转移性肿瘤的问题。
癌细胞可以从原发部位侵入淋巴管、血管,在其他部位形成转移性肿瘤,导致药物治疗靶标性效果并不理想。
这通常有助于癌症的扩散,而科学界也曾试图利用这一关键特性来提升治疗的效率。以往的研究包括:A.T.Power实验室利用癌细胞作为载体,在细胞中装入溶瘤病毒来杀灭癌细胞;J.García-Castro实验室则通过改造过的癌细胞,让其表达一些自杀基因从而向其旁侧癌细胞传输死亡信号;E. Dondossola实验室通过改造的癌细胞让其表达治疗性分子,抑制肿瘤血管的新生过程。
但这些方法都存在着或大或小的风险:癌细胞改造的过程本身让它们可能会有二次致瘤风险,造成更严重的后遗症。
但哈佛干细胞研究所(HSCI)的科学家已经找到了扭转局面的方法。
发表在《科学转化医学》(Science Translational Medicine)上的新研究显示,这些能自我定位的细胞可以被利用,将一种治疗分子直接送入肿瘤。
作者哈立德·沙阿(Khalid Shah)博士是HSCI的主要教员,Brigham妇女医院神经外科副主任,哈佛医学院副教授。
他表示:“该研究是攻关克难的一剂良方。在标准治疗手段中,向肿瘤靶向传送药物的失败率很高。我们的这项研究表明,通过逆编程手段,可以用病人本身的癌细胞来治疗癌症。我们认为这项技术可以延伸至所有的癌症类型。”
癌细胞的特性是无限增殖,而原本细胞正常的凋亡机制出了问题。这是一个问题的入手点,部分肿瘤细胞表面有一类肿瘤坏死因子(TNF)受体,也就是俗称的“死亡受体”。当特定的配体分子(肿瘤坏死因子相关凋亡诱导配体,TRAIL)与之结合,与凋亡相关的信号通路开启,就能结束癌细胞的无限增殖。
研究团队从中得到启示:他们使用CRISPR基因编辑技术,以天然不含TNF受体的癌细胞为载体,使该细胞在工程处理后能表达TRAIL蛋白分子。由于不含TNF受体,它们就能在保证自身安全的前提下,成为能够分泌TRAIL的肿瘤细胞杀手,对病人体内的肿瘤细胞造成伤害。
研究团队将这些细胞注射至患原发性成胶质细胞瘤小鼠的癌组织处。结果令人惊喜:它们分泌出的大量TRAIL与周围的肿瘤细胞结合,开启凋亡程序。在小鼠试验中,这种手段展现出了良好的效果。
针对原位癌的异源移植可以直接使用基因边际技术制造的不含TNF受体的肿瘤细胞,而针对复发转移癌,需要从病人癌组织中分离出含TNF受体的癌细胞,用过CRISPR介导的受体敲除技术,使得这些癌细胞不含TNF受体。
这种方式能利用癌细胞“自我归巢”的特性,让其跟踪已经扩散到同个器官或者身体其他部位的同伴。
在实验中,这种治疗方式也成功得到了验证,研究团队将来自小鼠自身的癌细胞经工程处理后重新注入患转移性成胶质细胞瘤的小鼠体内。研究团队观察到,这些细胞会直接向肿瘤区域迁移,并将周围的癌细胞杀死。这种方式使得患癌小鼠的生存率得到了显著提升。
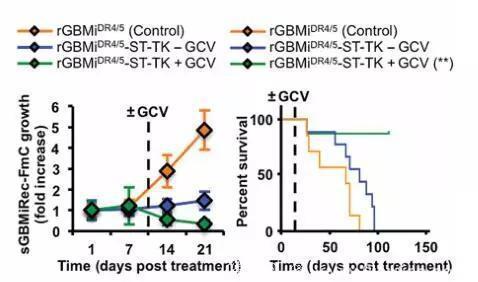
图:在肿瘤清除后消除工具细胞(图中绿色曲线)可以显著提升小鼠的生存率(约80%)。
但是,作为载体的工程癌细胞自身也不能被忽略,在杀死同类后,这些肿瘤细胞仍会不受控制地继续增殖。
因此:Shah和他的同事们还在这种载体癌细胞上设计了一种自毁机制:一种将药物转化为活性物质的蛋白质。
他们在工程癌细胞中加入药物前体转化酶,在清除肿瘤后,研究人员人为加入GCV试剂,这种酶会启动药物前体的转化,专门清除作为载体的癌症细胞。
“这项研究证明了工程肿瘤细胞对受体靶向治疗的潜力,”医学博士马里奥·苏瓦(Mario Suvà)说。
苏瓦博士是HSCI癌症项目的负责人,同时也是马萨诸塞州综合医院和哈佛医学院(HMS)的病理学助理教授。
他补充说:“这项研究展示了在HSCI癌症项目中正在研究的肿瘤生物学的许多独特方面,这些新发现可能会导致新的治疗策略。”
正如Shah在论文里所写的,“这种方法将为原位或者侵袭性转移癌的治疗提供无限的希望。”