肿瘤免疫领域六大投资机会

之前的放化疗、靶向药,都是用药物直接攻击肿瘤,肿瘤总是能较快进化出耐受药物的机制。肿瘤免疫治疗并不直接针对肿瘤,而是激活免疫系统抑制肿瘤的能力。
免疫系统能动态地、适应性地攻击肿瘤。免疫疗法改变了肿瘤治疗的格局,打开了通向把肿瘤变成慢性疾病的大门。
就肿瘤与免疫的关系而言,一方面免疫系统本来具有一定杀伤肿瘤细胞的能力;另一方面,这个杀伤能力不如杀伤细菌那样强大。
主要原因一是肿瘤来自人体,免疫原性不如外来入侵者;二是肿瘤发展出多种方式逃避、抑制免疫系统。
以这些方面的研究为基础,肿瘤免疫领域的新疗法逐渐出现,包括肿瘤疫苗、溶瘤病毒、细胞因子、细胞疗法、大、小分子药物疗法等,可以不同程度克服这两个因素,增强对肿瘤的杀伤。
其中药物治疗和细胞治疗近年来在临床上进展较为显著。本文的介绍只针对药物治疗部分。
下图用于帮助简要地了解已知的肿瘤抑制免疫细胞的方式,从而便于理解之后的药物机制:
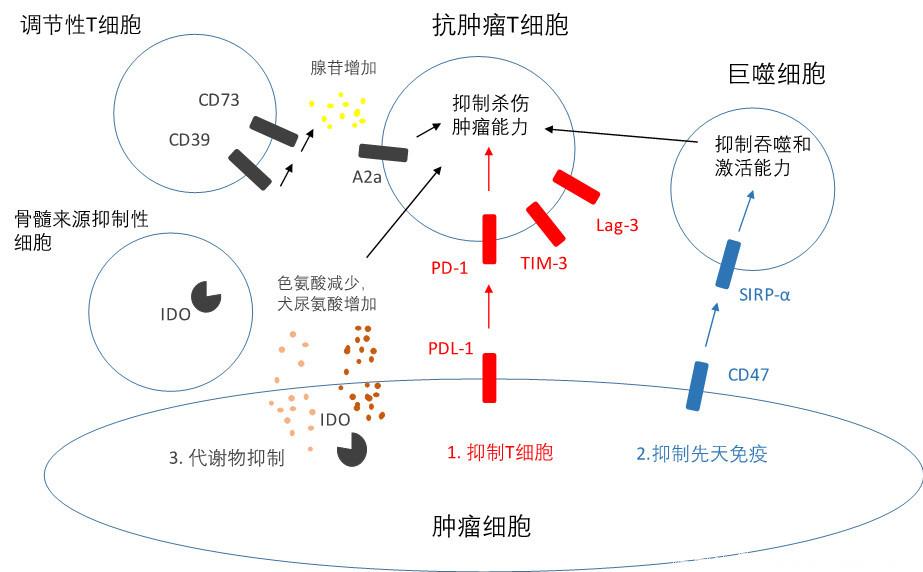
肿瘤细胞在局部形成特殊的微环境,还有骨髓来源抑制性细胞、调节性T细胞、肿瘤相关巨噬细胞等参与形成这个免疫抑制性环境。肿瘤微环境能抑制进入其中的T细胞的抗肿瘤活性。
抑制的主要方式具体来说包括:
- 1.抑制抗肿瘤T细胞:
- 如PD1/PD-L1通路就是典型代表。肿瘤细胞表达的PD-L1,结合T细胞表面的PD1分子,引起T细胞活性受到抑制。类似的靶点还有T细胞表面的Tim-3、Lag-3、TIGIT等分子。
- 相应的,药物设计的思路就是,通过药物分子,阻断PD-L1和PD1的结合,从而恢复T细胞杀伤能力;或者从另一个角度,T细胞表面还有激活性分子,通过药物分子结合,激活T细胞的杀伤能力。
2.抑制先天免疫细胞:
如肿瘤细胞表达CD47,与巨噬细胞等抗原递呈细胞表面的SIPR-α结合,避免被免疫细胞吞噬从而激活抗肿瘤T细胞。
相应的药物设计的思路就是,通过药物分子,阻断CD47和SIPR-α的结合,从而加强T细胞杀伤能力;或者从另一个角度,抗原递呈细胞表面还有激活性分子,通过药物分子结合来激活,从而增强T细胞的杀伤能力。
3.代谢物抑制举例:
a.肿瘤和骨髓来源抑制性细胞表达IDO、TDO,参与分解消耗色氨酸,产生犬尿氨酸。色氨酸缺乏导致抗肿瘤T细胞和NK细胞活性降低,犬尿氨酸可以促进其他免疫抑制机制。
b.调节性T细胞表达的CD73、CD39,产生腺苷。腺苷通过抗肿瘤T细胞上的A2a等受体,抑制抗肿瘤活性。
c.骨髓来源抑制性细胞表达的精氨酸酶,分解肿瘤局部的精氨酸,使精氨酸含量降低,抑制T细胞活性。
相应的药物设计的思路就是,通过药物抑制产生这些代谢物的酶,恢复抗肿瘤活性。

以下总结这个领域的药物研发进展:
- 1.已上市药物的进展
- 目前已经上市的药物有6个,总销售额2017年已经突破百亿美元。其中5个是针对PD1/PD-L1通路。PD1药物适应症较多,包括黑色素瘤、非小细胞肺癌、霍奇金淋巴瘤等;PD-L1药物主要是针对膀胱上皮癌和非小细胞肺癌。总体来看,这些药物显示了较好的疗效,为特定患者人群提供了相比以往更优的治疗方案。不过也存在一定局限:
- (1)整体有效率不高,各种肿瘤人群中对单药客观反应率一般不超过20-30%。
- (2)临床应用大都是针对晚期\复发\不可切除\转移性肿瘤,此时病人的病情已较严重。能否应用到更早期阶段,使更多患者获益,还有待研究。
- (3)效果还有待更多确认。目前作为一线用药方案的并不多,以Opdivo为例,目前只在黑色素瘤中获批用于一线治疗。
- 目前在临床上的科学探索,在这些局限点上有一定进展:
- (1)biomarker对病人分群:
- 找到最有可能有效的病人,让病人使用最可能从中获益的药物。比如使用肿瘤组织中PD-L1表达量为生物标记物,如果高于50%,才推荐使用Keytruda作为一线治疗。
- 目前已被FDA批准的用于肿瘤免疫药物的生物标记物包括PD-L1表达量、微卫星不稳定和肿瘤突变负荷程度。(2)探索新临床应用:延迟复发
- 对于III期非小细胞肺癌,在经过放化疗治疗控制住病情后,使用Imfinzi可以明显降低复发。在Pacific研究中,使用Imfinzi中位无进展生存期达16.8个月,安慰剂仅5.6个月。中晚期肿瘤的治疗,病人经常在复发后。
- 之前的肿瘤免疫药物在肺癌领域都是针对正在进展的肿瘤,而没有开拓预防复发的作用。Imfinzi在这一较大临床需求上实现了突破,对于患者延长生命和提高生活质量有重要的作用。
- (3)联合疗法改变一线治疗格局
- 通过与其他疗法的联合使用,提高疗效。具体在下面阐述。
- 2.联合治疗
- 鉴于已有的肿瘤免疫药物的局限性,联合疗法成为探索的热点。原理上主要是基于两点:
- 一是其他治疗可以杀死肿瘤细胞,使更多肿瘤抗原释放,联合PD1药物治疗,理论上可以增加杀伤;
- 二是肿瘤还存在除PD1之外的抗免疫机制,联合治疗可以抑制多个机制,理论上也可以增强抗肿瘤免疫,降低耐药。
- 根据Informa数据库信息,全球联合用药的临床试验中,两种肿瘤免疫药物联合的试验数目608个,肿瘤免疫与放化疗联合的试验532个,肿瘤免疫与靶向药联合的试验525个。
(1)肿瘤免疫药物相互联合使用
肿瘤免疫药物的联合用药试验取得了一些积极结果。其中BMS有两个上市药物Opdivo和Yervoy,所以进展较快。
这两个药物的联合,在非小细胞肺癌的CheckMate-227研究中,针对肿瘤突变负荷(TMB)高的人群,与标准化疗相比在无进展生存期上达到更优的临床终点,总体生存期仍在观察;在晚期肾癌的CheckMate-214研究中,对于中等和高等风险且PD-L1表达>1%的人群,联合疗法在客观反映率(58%对25%)和无进展生存期(22.8月对5.9月)达到终点,这个数据已获FDA优先评审,有望成为晚期肾癌的新疗法。
目前还有大量的肿瘤免疫领域未上市药物,这些药物的临床试验主要都是采用联合用药方案,这些药物会在后面章节叙述。
(2)在肿瘤免疫药物联合化疗的试验中,Keytruda和化疗联合已获批用于转移性非鳞非小细胞肺癌的一线治疗。
其他的尝试也正在进行。
(3)肿瘤免疫药物联合靶向药的试验中,呈现不同反应。
在联合EGFR、ALK突变的小分子靶向药时,发现效果并不好,而且还有多例死亡情况等严重安全性问题。在联合抗血管生成的靶向药时,显示出了积极的疗效。与其他药物的联合,如PARP抑制剂、HDAC抑制剂、MEK抑制剂、CD20靶点等等,也都在进行中。
3.未上市药物研发进展
目前重点研究的靶点及主要相关药物,按照机制类型分类列出如下:
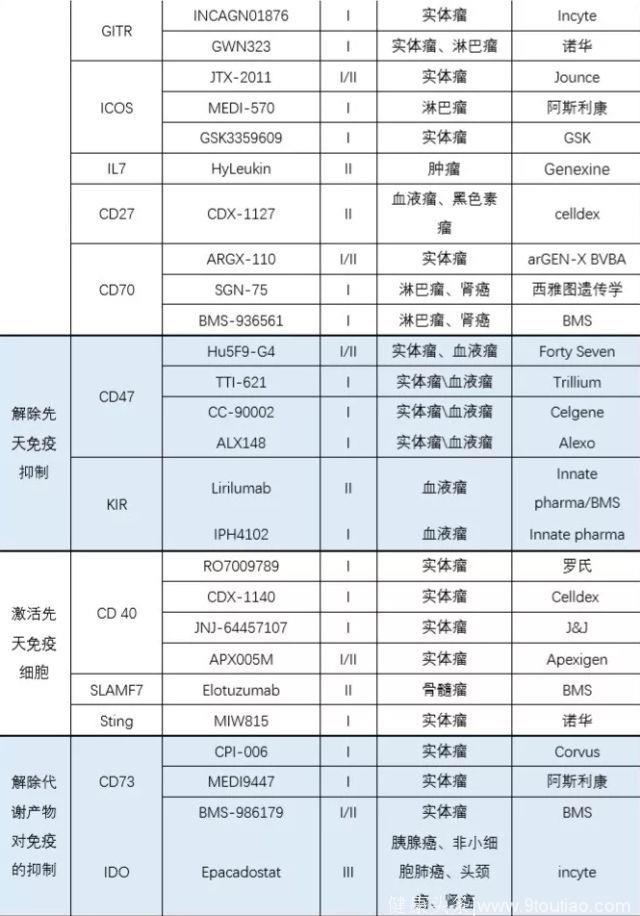
目前这些在研药物的临床试验基本都以探索联合用药为主。其中PD(L)-1药物是联合疗法的基石。联合用药另一种药物的选择,有的方案是选择另一种针对T细胞上靶点的药物,或是选择针对其他机制如先天免疫系统。

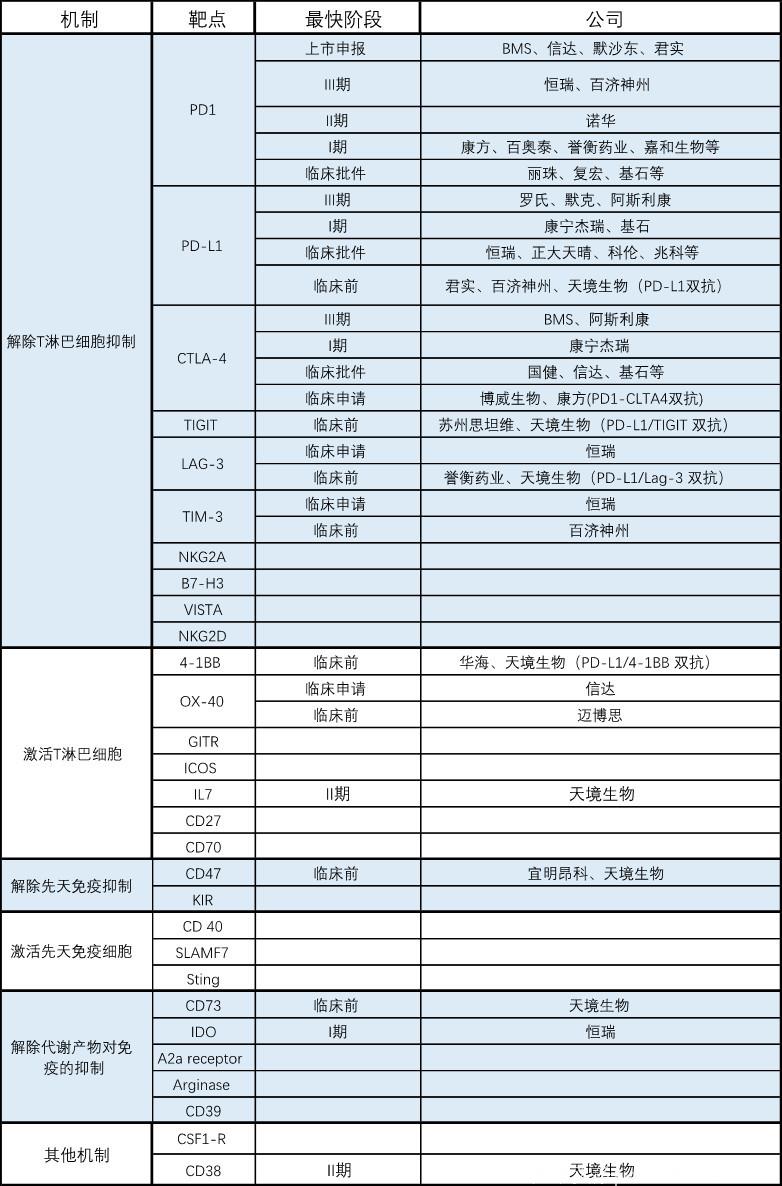
(信息持续更新中)
国内在肿瘤免疫领域的布局,以跟随国外为主,且主要集中在少数几个靶点。特别是PD1和PD-L1,国内开发企业较多。其他靶点,国内开发进度较慢。
下表是从Insight数据库整理的对PD1药物进度最快的4家公司在国内临床试验的总结:
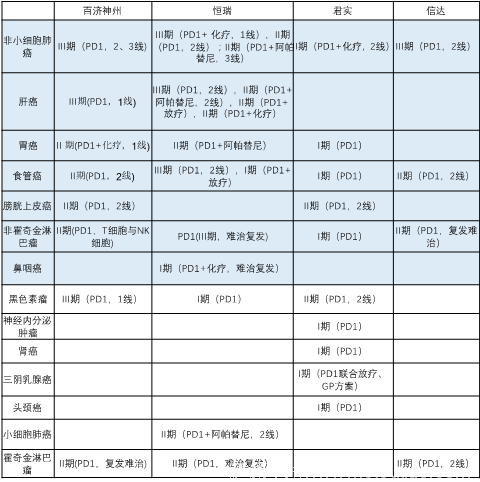
(标蓝色的为我国死亡率排名前12的癌症)
可以看到,恒瑞和百济神州的PD1药物适应症基本覆盖了市场较大的癌症,同时进度也更为领先。例如恒瑞在前两大癌症,注册了多个临床试验,包含了各种联合疗法,试图最大化占领市场。
这种情况下,如何布局寻求立足,是后来者需要仔细考虑的。主要可能的方向包括:
一是对抗体分子的改造优化,丰富其功能,或降低不良反应;
二是探索新靶点,新适应症,特别是要结合生物标记物研究个体化治疗;
三是探索新的联合治疗方案。
四、总结
- 肿瘤免疫原理仍有很多需要探索,未来价值值得期待。
- 2.目前的临床研究方向主要在优化药物使用、探索联合疗法和寻找新的药物。 3.国内的公司布局集中在PD(L)-1靶点,但还有许多值得开拓的机制和靶点。
- 对于布局肿瘤免疫领域的创新药企业,有以下几点可以重点考察:
- (1)团队
- 核心团队完整,具备深厚科学研究基础、丰富的药物全流程研发能力、尤其是临床研究经验以及国际合作能力。
- (2)产品线
- 目标公司要有能力在科学认识基础上提前布局靶点。肿瘤免疫涉及先天免疫、获得性免疫、代谢等多个途径,还可以联合其他疗法。所以需要了解创始人对其开发靶点之科学依据的认识。另外产品研发进度在同类中较领先。
- (3)市场情况
- 主要包括分析具体适应症人群大小、现有疗法、目前存在的未满足临床需求、医生用药观念、支付意愿、支付能力等。优秀公司能发掘目前仍存在的未满足重大临床需求,针对性地开发药物。
/高特佳原创研报