免疫学视角丨转移性葡萄膜黑色素瘤的治疗(二)
导读
葡萄膜黑色素瘤是比较罕见的疾病,但却是成年人最常见的原发性眼内恶性肿瘤。最常转移的部位是肝脏,患有该种疾病的患者中,很少能通过手术来达到好的治愈效果,因此也导致该疾病预后不良。
葡萄膜黑素瘤(UM)是成人最常见的原发性眼部恶性肿瘤,多达50%的患者在最佳治疗后发生了全身转移。UM的恶性程度极高,短期内可蔓延至眼眶、颅内,或经血行转移至全身脏器,以肝脏转移最常见。UM一旦发生转移,致死率极高。对于已经发生转移的UMM患者,尚无有效的治疗。
当前UM免疫治疗方法
皮肤黑色素瘤(CM)与UM之间的主要区别在于突变负荷,即相较于CM的高突变负荷,UM具有较低的突变负荷。转移性UM对于常规全身性化疗具有高度抵抗性,目前获批用于CM的信号抑制剂并不适用于转移性UM。另外,肝脏是最致耐受性的免疫微环境之一。转移性UM是最具挑战性的肿瘤之一,全身性和局部治疗的生存获益仍有待观察。目前已开展多项应用免疫疗法治疗转移性UM的临床试验。这些临床试验提供了剖析转移性UM的免疫微环境的重要视角,并明确了转移性UM免疫治疗的未来研究方向。
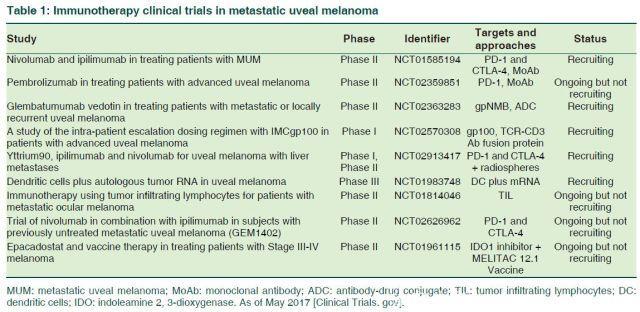
局部治疗
肝脏是UM转移的首个且重要的部位,因此局部治疗可直接破坏肿瘤,并启动全身免疫系统损害肿瘤相关抗原。目前,研究人员研发了一种称为“免疫栓塞(IE)”的方法。理论上,栓塞缺血效应将杀伤转移性UM细胞;GM-CSF刺激APC并促进肿瘤抗原摄取,诱导肝脏和次级淋巴结中的T细胞活化。这种方法可能导致全身抗黑色素瘤免疫力发展,延缓肝外转移的发展和进展。一项临床试验验证了这一概念。相较于1,3-双(2-氯乙基)-1 -亚硝基脲(CE)化疗栓塞,IE可显著诱导更高的总生存期(OS)[20.4 vs. 9.8个月, P=0.005]和无进展生存期(PFS)[12.4 vs. 4.8个月, P=0.001]。
在随后进行的双盲临床试验中,研究人员比较了肝肿瘤乙碘油生理盐水溶液“轻度栓塞(BE)”与IE。IE组总生存期为21.5个月(95%CI:18.5-24.8个月),BE组为17.2个月(95%CI:11.9-22.4个月)。IE治疗后促炎细胞因子产生程度更强。IE处理后1h和18h,患者血清中TNF-α,IL-6和IL-8水平均升高。另一方面,BE处理后18h,患者血清中IL-6和IL-8水平轻度升高。IE处理后细胞因子更高程度释放与更长“系统性”肝外进展时间相关。IE组中,处理后1h较高水平IL-6(p<0.001)和18h较高水平IL-8(p<0.001)是较长系统PFS的重要预测因子。目前,研究人员正在启动一项新的II期研究,该研究将IE与免疫检查点抑制剂ipilimumab和nivolumab联用。
由于大多数患者的肝转移受生命限制,传统化疗或免疫治疗难以诱导抗肿瘤反应,因此研究人员研发了多种肝靶向治疗方案,如经皮肝灌注+美法仑,肝动脉灌注+福莫司汀。然而,肝靶向治疗对肝脏肿瘤免疫微环境的影响仍有待研究。
全身免疫治疗
1
免疫检查点抑制剂
抗细胞毒性T淋巴细胞相关抗原4(CTLA-4)和PD-1/PD-L1抗体的研发和获批为转移性UM患者带来了新的治疗模式和希望。然而,这种新方法并未改善转移性UM患者的结局。既往研究表明,抗CTLA-4和抗PD-1/PD-L1抗体在转移性UM患者中的应答率差强人意。一项回顾性研究收集了82例ipilimumab治疗的可评估UM患者的数据,每3周3 mg/kg,最大4个剂量CTLA-4全人源化单抗治疗后,4 (5%)例患者出现免疫相关客观缓解,24(29%)例出现持续3个月以上的免疫相关稳定疾病期。中位随访5.6个月,中位OS为6.0个月,中位PFS为3.6个月。1年OS和PFS率分别为31%和11%。
另外一项回顾性研究纳入了34例3 mg/kg ipilimumab和5例10 mg/kg ipilimumab治疗患者。研究表明,1例患者获得完全缓解(CR),1例患者获得晚期部分缓解(PR),免疫相关缓解率为5.1。3 mg/kg ipilimumab组的OS为9.6个月(95%CI:6.3-13.4个月)。本研究的生存期范围为1.6〜41.6个月。回顾性研究中的56例抗PD-1/PD-L1抗体治疗患者也表现出了令人失望的反应。56例UM患者中,仅2例表现出客观肿瘤反应(OS为3.6%[95%CI:1.8-22.2%]),5例患者病情稳定(≥6个月)。中位PFS为2.6个月(95%CI:2.4-2.8个月),OS为7.6个月(95%CI:0.7-14.6个月)。相较于非肝转移CM,该研究结果可能与转移性UMPD-L1低表达相关。值得一提的是,肝转移性CM患者抗PD-1抗体治疗应答也很差。这进一步支持了“肝脏免疫微环境阻碍了抗癌T细胞免疫应答”的假设。
2
肿瘤浸润T细胞过继免疫疗法
肿瘤浸润性T细胞(TIL)疗法可以成功治疗转移性UM治疗,获得持续反应以及大量转移消退。国立癌症研究所开展的一项II期临床研究纳入了21例经TIL疗法治疗的HLA-A2阳性转移性UM患者。在20名可评估患者中,7名患者出现肿瘤消退,其中6名患者获得PR,一名患者获得CR。应答者和无应答者的肿瘤突变负荷无显著差异。另一方面,小于3%,或少于2×109的肿瘤反应性T细胞,或少于100 pg/mL的肿瘤诱导性IFN-γ释放的TIL产物引发了不良临床反应。该研究表明,自体TIL过继性转移可以介导转移性UM患者客观肿瘤消退。
3
DC疫苗
黑素细胞相关蛋白(如gp100,MART-1,酪氨酸酶和TRP-1)也表达于大多数人UM。这些肿瘤相关抗原构成了转移性疾病免疫治疗的合适靶标。DC是抗原呈递细胞,具有激活初始T细胞的独特功能,因此适用于诱导免疫抗肿瘤反应。一项研究应用负载gp100和酪氨酸酶的治疗性DC疫苗治疗了14名转移性UM患者。入组标准为患者具有HLA-A*02:01表型或HLA-DRB*01:04,并且必须为表达gp100和酪氨酸酶的转移性UM。所有患者均以各种方式(突变型或野生型肽,或mRNA)接种3次负载gp100和酪氨酸酶的自体DC疫苗(每2周一次)。最后一次接种后1~2周进行皮肤测试。在无疾病复发情况下,患者每隔6个月接种最多2次维持期疫苗。DC疫苗接种后,在4(29%)名患者中检测到gp100和酪氨酸酶特异性T细胞。接种DC疫苗的转移性疾病患者的中位总生存期为19.2个月,未见严重治疗相关不良事件(常见毒性标准3或4级)。临床未见转移病灶消退。然而,这种治疗性DC疫苗的疗效仍有待进行大规模前瞻性研究。
4
TCR和抗CD3抗体融合蛋白
IMCgp100是包含gp100特异性T细胞受体(HLA-A * 02:01)和抗-CD3 scFv的融合蛋白。IMCgp100与MHC I类分子上表达gp100肽的UM细胞结合,然后通过抗CD3抗体给另一端附加CD3+T细胞。加工和修饰后的可溶性TCR与HLA-A*02:01分子上的gp100肽具有极高的亲和力。早期临床研究得出了积极的结果,研究人员将开展一项关于转移性UM的大规模随机II期研究。
5
靶向糖蛋白NMB的抗体
Glembatumumabvedotin(也称为CDX-011和CR011-vcMMAE)是一种靶向表达跨膜糖蛋白NMB(gpNMB)癌细胞的抗体-药物缀合物(ADC)。它是含有抗gpNMB全人IgG2单抗和细胞毒性药物单甲基奥瑞他汀E(MMAE)的融合分子。抗gpNMB抗体与表达肿瘤细胞的gpNMB结合,内化后,抗体会释放MMAE。多种肿瘤(如黑色素瘤和乳腺癌)过表达gpNMB。
总结
转移性UM的治疗疗效可能非常有限,而诱导抵抗UM细胞的免疫力可能是最大的挑战。特殊条件可以产生抗癌免疫反应,如存在认知抗原,APC水平升高,高亲和力交互式TCR,肝脏中抑制性免疫细胞或分子消耗。鉴于潜在的预存在抗UM细胞免疫耐受性,低突变负荷以及肝脏中的免疫调节微环境,应用免疫刺激分子扰乱肝转移或肝转移后进行免疫刺激分子机械扰乱可能是合理的治疗方案。
另外,正如正在进行的临床试验所建议,体外活化的肿瘤特异性T细胞或模拟诸如双特异性融合蛋白方案将是抗转移UM最具前景的治疗方法。转移性UM特有的关键信号通路抑制剂可能也有助于增强UM细胞的免疫原性,反过来提高当前免疫检查点抑制剂的功效。研发更有效的抗转移性UM免疫治疗策略可能需要基础免疫学研究者与临床科学家进行进一步合作。
文章编译自:Mizue Terai, Michael J. Mastrangleo, Takami Sato.J Cancer Metastasis Treat.Immunological aspect of the liver and metastatic uveal melanoma.2017;3:231-43.
1.免疫学视角丨转移性葡萄膜黑色素瘤的免疫微环境(一)
2.肿瘤免疫检查点治疗“拦路虎”之肿瘤微环境篇
3.免疫治疗联合放射治疗的过去、现在与未来